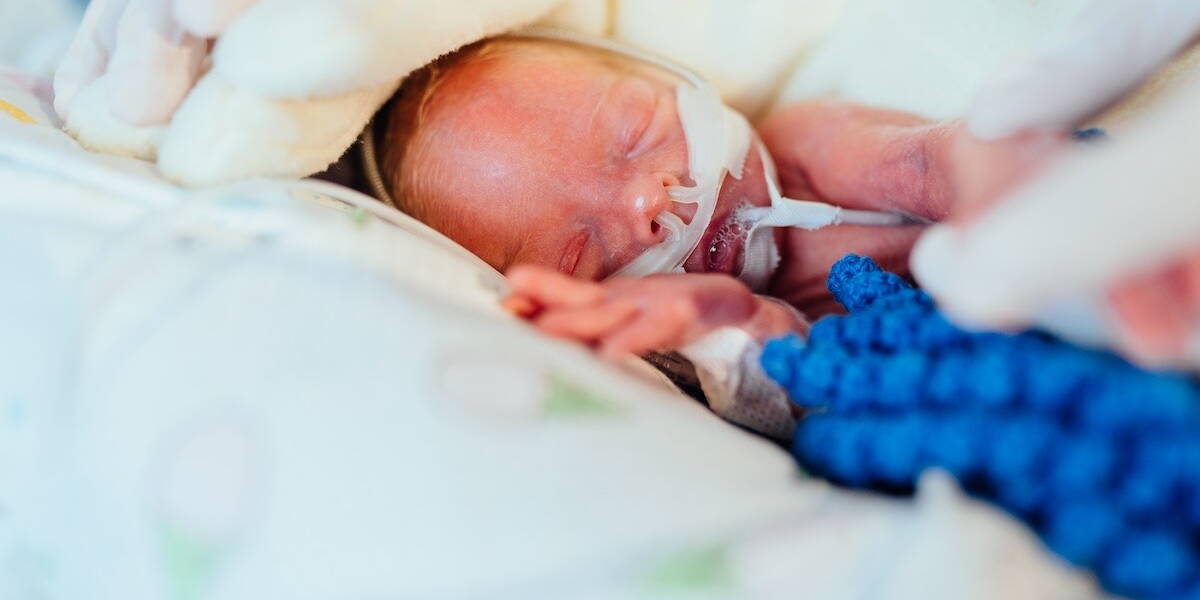
Onderzoekers in Zweden hebben een in het laboratorium gekweekt menselijk hersenmodel ontwikkeld dat kan helpen hersenbeschadiging bij premature baby's te voorkomen. Met behulp van dit geavanceerde systeem konden wetenschappers voor het eerst observeren hoe hersenbloedingen neurale stamcellen beïnvloeden tijdens vroeggeboorte en een mogelijke behandeling testen die de schade aanzienlijk verminderde. Het onderzoek werd geleid door teams van het KTH Royal Institute of Technology, het Karolinska Institutet en de universiteiten van Lund en Malmö.
Intraventriculaire bloeding (IVH) is een van de ernstigste neurologische complicaties bij premature baby's. Wanneer rode bloedcellen in de subventriculaire zone (SVZ) van de hersenen lekken en afbreken, geven ze ontstekingsmoleculen vrij, zoals interleukine-1 (IL-1). Deze immuunsignalen zorgen ervoor dat neurale stamcellen hun flexibiliteit verliezen en voortijdig veranderen in andere celtypen, of helemaal stoppen met ontwikkelen.
“In plaats van klaar te blijven om uit te groeien tot verschillende hersencellen, beginnen de stamcellen te vroeg te veranderen of stoppen ze helemaal met groeien”, legt professor Anna Herland, hoofddocent aan het AIMES-onderzoekscentrum (een gezamenlijk initiatief van KTH en Karolinska), uit. “Dit verstoort de ontwikkeling van de hersenen en verhoogt het risico op langdurige neurologische schade.”
Een baanbrekend model
Tot nu toe waren de meeste studies naar IVH gebaseerd op diermodellen, die slechts gedeeltelijk de biologie van het menselijk brein weergeven. Om die kloof te overbruggen, werkte het Zweedse onderzoeksteam samen met de Ege Universiteit in Turkije en Harvard University om een in-vitromodel te bouwen met behulp van menselijk stamcel-afgeleid hersenweefsel. Dit “minihersenen” bootst nauwkeurig na hoe menselijke neurale stamcellen en gliacellen reageren op bloedingen in de hersenen, en biedt een nieuwe manier om ontstekingen en weefselherstel te bestuderen.
Herland noemt het “een van de meest complexe en realistische in-vitro hersenmodellen die ooit zijn ontwikkeld”. Het stelde het team in staat om voor het eerst een gericht tegengif te testen, een IL-1-antagonist, die de ontstekingsreactie met succes verminderde en gedeeltelijke bescherming bood aan neurale stamcellen. De studie is onlangs gepubliceerd in Advanced Science.
Betere therapieën voor premature baby's
De onderzoekers analyseerden ook het hersenvocht (CSF) van baby's met een hersenbloeding. Ze ontdekten dat CSF weliswaar vergelijkbare cellulaire veranderingen veroorzaakte, maar dat de effecten milder waren vanwege lagere toxineconcentraties en de aanwezigheid van beschermende voedingsstoffen en ontstekingsremmende eiwitten.
De resultaten van het onderzoek betekenen een belangrijke stap in de richting van het vinden van veilige, effectieve behandelingen voor hersenletsel bij premature baby's. “Er is momenteel geen beproefde therapie voor deze baby's”, zegt Herland. “Met ons model kunnen we mogelijke interventies testen in een voor de mens relevant systeem, zonder de veiligheid van patiënten in gevaar te brengen. Vervolgens willen we het model uitbreiden om verschillende niveaus van letsel te simuleren en meer veelbelovende geneesmiddelen te testen.”
Met zijn combinatie van precisie-bio-engineering en klinische relevantie zou deze doorbraak kunnen helpen de neonatale geneeskunde te transformeren en nieuwe hoop bieden voor de bescherming van de meest kwetsbare patiënten tegen levenslange neurologische schade.
Brain-on-a-chip
Enkele weken geleden berichtten wij over een innovatieve brain-on-a-chip-technologie die het mogelijk maakt om te onderzoeken hoe het brein zichzelf beschermt en waarom dat soms misgaat bij aandoeningen zoals sepsis of neurodegeneratieve ziekten. In plaats van dierproeven gebruiken de onderzoekers microchips met menselijk weefsel om de werking van de bloed-hersenbarrière te bestuderen, de cruciale scheiding tussen bloed en hersenen.
De wetenschappers van de University of Rochester zijn voornemens hun model uit te breiden met microgliacellen om beter te begrijpen hoe hersencellen reageren en hopen de technologie uiteindelijk te kunnen gebruiken voor gepersonaliseerde behandelstrategieën.