Wetenschappers van het European Molecular Biology Laboratory (EMBL) in Heidelberg hebben een innovatieve AI-technologie ontwikkeld die een doorbraak betekent in het begrijpen van hoe kanker ontstaat. Het nieuwe systeem, genaamd MAGIC combineert AI, geautomatiseerde microscopie en lasertechnologie om afwijkende cellen automatisch te identificeren, markeren en analyseren.
Deze techniek maakt het mogelijk om het proces van celdeling en de eerste stappen richting kankerontwikkeling op ongekende schaal te bestuderen. MAGIC staat voor Machine learning-Assisted Genomics and Imaging Convergence.
Chromosomale afwijkingen
Kanker ontstaat wanneer de genetische instructies in een cel verstoord raken. Door opeenstapeling van DNA-fouten kunnen cellen de controle over hun groei verliezen en zich ongecontroleerd gaan delen. Chromosomale afwijkingen, structurele of numerieke defecten in chromosomen, vormen vaak de eerste stap in dit proces. Zulke afwijkingen worden geassocieerd met agressieve kankersoorten en dragen bij aan uitzaaiingen, therapieresistentie en een verhoogde kans op terugkeer van tumoren.
“Chromosomale afwijkingen zijn een belangrijke motor achter agressieve vormen van kanker en worden sterk gelinkt aan metastase, therapieresistentie en vroege tumorgroei,” zegt professor Jan Korbel, senior onderzoeker bij EMBL en hoofdauteur van de studie. “We wilden begrijpen hoe vaak zulke afwijkingen ontstaan wanneer normale cellen zich delen, en welke factoren dat risico verhogen.”
Het idee dat chromosoomafwijkingen kunnen leiden tot kanker is niet nieuw. Al ruim een eeuw geleden opperde de Duitse wetenschapper Theodor Boveri dat een verkeerde chromosomale samenstelling in een cel de basis kon vormen voor tumorontwikkeling. Toch bleek het buitengewoon moeilijk om dit proces in detail te bestuderen: slechts een klein deel van de cellen vertoont op enig moment zulke afwijkingen, en deze cellen sterven vaak snel af. Het handmatig opsporen en analyseren van zulke cellen onder de microscoop was een tijdrovende en foutgevoelige klus.
‘Laser tag’ voor kankercellen
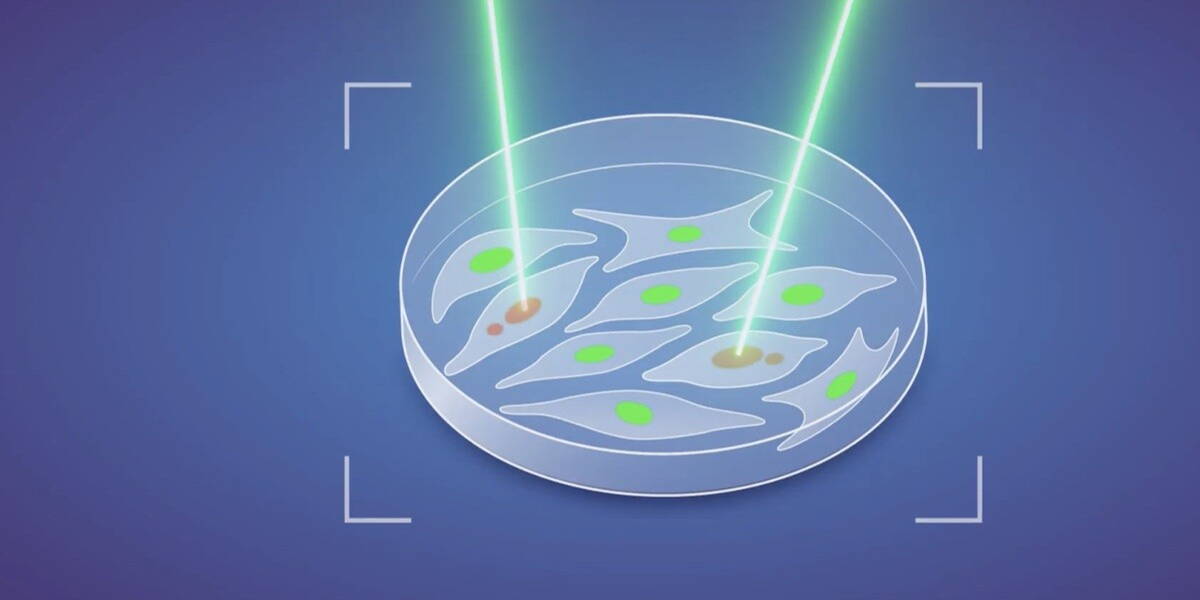
Daar brengt MAGIC verandering in. Het systeem werkt als een geautomatiseerde versie van een potje ‘laser tag’: het zoekt en markeert cellen met een specifieke eigenschap. In dit geval richtten de onderzoekers zich op micronuclei. De kleine DNA-bevattende blaasjes in de cel die wijzen op fouten in de celdeling en een voorbode zijn van chromosomale instabiliteit.
MAGIC gebruikt kunstmatige intelligentie om deze micronuclei automatisch te herkennen op microscopische beelden. Zodra de AI een verdachte cel detecteert, stuurt het systeem een laser aan die de cel “tagt” met een fotoconverteerbare kleurstof. Deze kleurstof verandert van kleur wanneer er licht op valt, zodat onderzoekers precies kunnen zien welke cellen afwijkingen vertonen. Deze gelabelde cellen kunnen vervolgens geïsoleerd en verder onderzocht worden met technieken zoals single-cell sequencing.
“Het mooie aan dit systeem is dat het meerdere disciplines samenbrengt,” vertelt dr. Marco Cosenza, onderzoeker in de Korbel Group en eerste auteur van de studie die gepubliceerd is in Nature. “Genomica, microscopie en robotica komen hier samen. Dankzij AI kunnen we nu in minder dan een dag tienduizenden cellen analyseren. Iets wat vroeger weken kostte.”
Nieuwe inzichten in tumorvorming
Met behulp van MAGIC analyseerden de onderzoekers duizenden menselijke cellen en ontdekten dat bij ongeveer 10 procent van alle celdelingen spontaan chromosomale afwijkingen ontstaan. Wanneer het p53-gen, een bekend tumorsuppressorgen, beschadigd is, verdubbelt dat percentage bijna. Deze bevinding bevestigt dat genetische instabiliteit al in een vroeg stadium kan optreden en een cruciale rol speelt in het ontstaan van kanker.
Daarnaast bracht MAGIC nieuwe informatie aan het licht over hoe DNA-breuken bijdragen aan deze afwijkingen. Door de precieze locatie van dubbelstrengs DNA-breuken in chromosomen te bestuderen, konden de onderzoekers zien hoe fouten in DNA-herstel leiden tot structurele veranderingen. Inzichten die van groot belang zijn voor het ontwikkelen van gerichtere therapieën.
Brede toepasbaarheid
Het onderzoek werd uitgevoerd in samenwerking met onder meer het German Cancer Research Centre (DKFZ) en de Universiteit van Heidelberg. Volgens de onderzoekers is MAGIC niet alleen geschikt voor kankerstudies, maar ook voor andere vormen van biomedisch onderzoek waarbij celafwijkingen een rol spelen.
“Zolang een afwijking visueel te onderscheiden is van een normale cel, kan het systeem dankzij AI getraind worden om die te herkennen,” aldus Korbel. “Dat maakt MAGIC buitengewoon veelzijdig en toepasbaar in talloze onderzoeksgebieden, van genetische ziekten tot nieuwe medicijnontwikkeling.”
Door het proces van celherkenning te automatiseren en te koppelen aan kunstmatige intelligentie, biedt MAGIC een geheel nieuwe manier om het ontstaan van kanker te onderzoeken, snel, nauwkeurig en op menselijke schaal. Daarmee brengt deze technologie onderzoekers een stap dichter bij het ontrafelen van de allereerste momenten waarop gezonde cellen transformeren tot kankercellen.